Para la dispepsia
Nota: Los fármacos descritos en este apartado deben ser prescritos y supervisados por un médico, preferentemente, un especialista en aparato digestivo. Aquí un listado de digestivos recomendados.
Aunque la dispepsia está catalogada por el grupo de Roma como un trastorno funcional distinto del SII, la realidad es que hasta el 50% de pacientes con SII pueden presentar también un diagnóstico de dispepsia funcional (ver 3.1.3, comorbilidad). Por eso hemos incluido un breve apartado con orientaciones básicas de su manejo.
Cuando hay dispepsia funcional (criterios diagnósticos aquí), el tratamiento es el mismo que para la gastritis (ver 3.3.), aunque pueden diferenciarse 2 grupos: los que tienen dolor epigástrico, tratados con IBPs, y los que tienen dolor/molestia posprandial (dolor tras las comidas), tratados con procinéticos como la mosaprida o la acotiamida. Otro procinético que se ha empleado es la metoclopramida (el clásico «Primperan», eficaz para las náuseas, vómitos y acelerar el vaciamiento gástrico), y recientemente se ha visto que el IberoGast podría ser incluso más eficaz que ésta (IberoGast es un medicamento que, entre otras cosas, influye sobre el tono de la musculatura lisa del tracto digestivo, pero lleva ingredientes con alto contenido en FODMAPs como manzanilla y regaliz, que pueden sentar mal si también se sufre un SII). En casos resistentes al tratamiento se han utilizado también antidepresivos (tricíclicos como amitriptilina, ISRS), de hecho, una revisión de 2017 señalaba a los antidepresivos tricíclicos y antipsicóticos como las medicaciones psicotrópicas más efectivas para la dispepsia (aunque con un éxito muy limitado), por su efecto neuromodulador. Una opción poco investigada pero que parece que a algunos les da resultado, es seguir la dieta low FODMAP, igual que los pacientes con SII. Sin embargo, la efectividad de esta dieta en la dispepsia no está del todo clara, y hay que tener en cuenta que la dispepsia no suele cursar con tantas intolerancias como el SII o los trastornos funcionales intestinales (probablemente, aunque esto es una suposición, porque el estómago tiene un número muy reducido de bacterias en comparación con el colon, lo que reduce las posibilidades de fermentación y acúmulo de gases, entre otros problemas). AQUÍ un artículo con recomendaciones dietéticas para la dispepsia.
En este enlace quizá encontréis más información, pero aporta poco a lo que acabamos de comentar.
Aquí tenéis la «Guía de Práctica Clínica sobre el manejo del paciente con Dispepsia Funcional» de la AEG, actualización de 2012, que incluye un breve esquema de tratamiento:
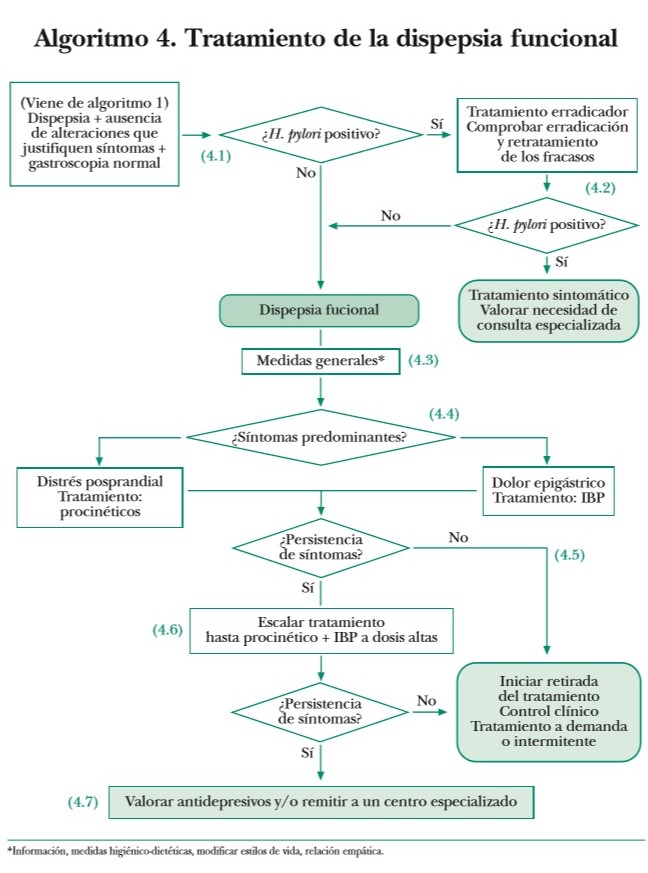
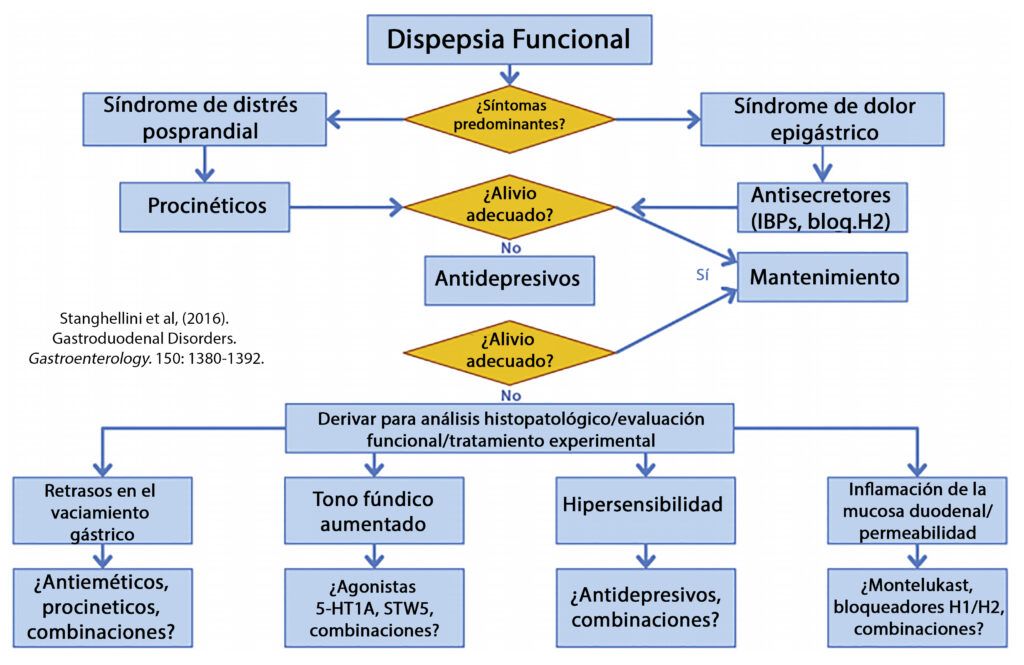
Una revisión de 2018 de la Rome Foundation muestra evidencia preliminar en el uso de azapironas (como la buspirona o la tandospirona) para aumentar las contracciones esofágicas y mejorar la acomodación gástrica de la comida, lo que mejoraría síntomas como la saciación temprana, la sensación de llenazón, o la náusea, y de antipsicóticos atípicos (aripiprazol, levosulpirida, olanzapina, quetiapina, sulpirida) para reducir el dolor epigástrico (en el caso de las sulpiridas, también las proponen para mejorar las náuseas). Sin embargo, el mayor grado de evidencia para el dolor epigástrico sigue correspondiendo a los antidepresivos tricícilicos (amitriptilina, imipramina, nortriptilina).
En otro estudio del mismo año y del mismo autor principal, se hacen algunas propuestas sobre el tratamiento de la dispepsia funcional (en la variante del síndrome de distrés posprandial) y las posibles combinaciones entre diferentes neuromoduladores para tratarla. La combinación principal según este artículo (aunque depende de cada caso) es la de buspirona, mirtazapina, y un antidepresivo tricíclico, aunque resulta extraño, considerando que la mirtazapina no se suele recomendar en combinación con tricíclicos por el elevado riesgo de interacciones.
Respecto a la duración del tratamiento, cuando se utilizan fármacos neuromoduladores como antidepresivos, antipsicóticos, o antiepilépticos, se recomienda un tiempo mínimo de 6-12 meses, y JAMÁS se debe suspender de golpe sin antes consultar al médico. Los ansiolíticos (incluyendo aquí las azapironas), a diferencia de los anteriores, tienen efecto casi inmediato y no se aconsejan en tratamientos largos por su potencial adictivo, aunque esto puede depender de la persona, el problema a tratar y la dosis empleada.
A la hora de suspender un antidepresivo (aunque esto puede aplicarse a cualquier otro neuromodulador) que hemos mantenido durante un cierto tiempo, las guías clínicas a veces recomiendan una discontinuación breve, con reducciones progresivas de la dosis durante 2-4 semanas hasta dejarlo del todo. Si no se hace así, puede aparecer un fenómeno llamado síndrome de discontinuación (o abstinencia, si hablamos de ansiolíticos), con síntomas muy variopintos que a veces se pueden confundir con recaídas. Sin embargo, algunos pacientes necesitan más tiempo, y, de hecho, estudios recientes en revistas de alto impacto (2019, 2020, 2020) van en esta misma línea, defendiendo una discontinuación más alargada en el tiempo y adaptada a las necesidades del paciente.
En cuanto a los procinéticos, pueden utilizarse tanto a corto como a largo plazo, y se pueden suspender en cualquier momento. Y en lo que respecta a los IBP, también se pueden usar a corto y a largo plazo, pero si se dejan, se recomienda hacerlo de manera paulatina y siguiendo las indicaciones de un médico. Un estudio de 2017 en Nature Reviews destacó algunos riesgos del uso continuado de IBPs, de los cuales sólo había relación causal confirmada para: aumento de infecciones gastrointestinales, cambios funcionales y estructurales de la mucosa gástrica, y daño renal agudo.
