Para el dolor
Nota: Los fármacos encuadrados en la categoría de «medicamentos» deben ser prescritos y supervisados por un médico, preferentemente, un especialista en aparato digestivo o un especialista de la Unidad del Dolor. Aquí un listado de digestivos recomendados.
Es el síntoma central y definitorio de este síndrome, y probablemente el más molesto e insidioso. El dolor, en personas sanas, suele ser una señal de que algo no marcha bien. Sin embargo, en el SII no hay lesiones aparentes, no hay cáncer de colon, no hay EII, no hay inflamación en el páncreas o cálculos en la vesícula, ni otros problemas visibles…y cuando los hay, los síntomas siguen siendo excesivos y el diagnóstico resulta insuficiente para explicarlos. En el SII, el dolor no nos avisa de nada, o al menos, nada que pueda poner en peligro la propia vida o provocar daños físicos en nuestro intestino. Por tanto, el dolor aquí es un mecanismo desadaptativo y disfuncional, y el tratamiento debe ir dirigido a suprimirlo en la medida de lo posible.
Con respecto a la localización de este dolor, ocurre en el colon, y no se extiende al intestino delgado, aunque en un porcentaje alto de pacientes el dolor también ocurre en áreas como el estómago (dispepsia funcional), y en un porcentaje menor puede coincidir con otros tipos de dolor, por ejemplo dolor musculoesquelético generalizado (fibromialgia).
Respecto a su cualidad, no es un dolor nociceptivo (el que se produce cuando un tejido sufre un daño y la señal de dolor llega al cerebro, es el que sentimos al darnos un golpe, ser picados por una abeja o hacernos una quemadura, y responde bien a antiinflamatorios y analgésicos como ibuprofeno o paracetamol), y tampoco es exactamente un dolor neuropático (el que se produce por un daño al propio sistema nervioso, central o periférico, y que suele expresarse como una sensación de hormigueo, quemazón o hipersensibilidad). El SII se ha englobado históricamente como un subtipo de dolor nociceptivo denominado dolor visceral (que viene de los nociceptores de las vísceras), en contraposición al subtipo somático (que viene de la piel, músculos, tendones o huesos). Otras clasificaciones lo consideran como un dolor «central», es decir, un dolor que proviene en gran medida del SNC. El gran problema es que es posible que haya tantos tipos de dolor como mecanismos implicados en su origen. En el SII son frecuentes los pinchazos o punzadas en zonas muy localizadas, la sensación de presión propia del dolor cólico, la quemazón, los calambres que recorren un área del colon como un latigazo…
El dolor puede estar muy asociado a síntomas como la diarrea/estreñimiento o los gases, es por esto que, antes que nada, habría que intentar controlar estos síntomas, y ver si con ello el dolor mejora. También puede darse el caso contrario, por ejemplo, hay pacientes SII-E que notan que ir más al baño contribuye a empeorar su dolor.
Una vez hecho esto, los tratamientos actuales son…
MODIFICACIONES DIETÉTICAS
Los mejores resultados se consiguen con la dieta low FODMAP ya mencionada, que mejora los síntomas en un 70% de pacientes aproximadamente. Algunos pacientes también se benefician de algunas pautas de la dieta NICE como reducir las grasas y las bebidas carbonatadas/estimulantes, o respetar los horarios y hacer 5-6 comidas al día, evitando las comidas copiosas, comiendo tranquilos y masticando bien los alimentos. El exceso de fibra también podría dar problemas en algunos casos, incluso en alimentos bajos en FODMAPs. Sin embargo, puede que no sea suficiente sólo con la dieta, y para eso hay ciertos fármacos que podrían ayudar.
MEDICAMENTOS*
- Antiespasmódicos: Uno de los tratamientos más frecuentes, se utilizan principalmente cuando el dolor es leve/moderado y ocurre de manera esporádica (nota de los administradores: los antiespasmódicos suelen funcionar mejor con el dolor de tipo cólico/presión, cuando el dolor adquiere características neuropáticas como quemazón, se ven mejores resultados con neuromoduladores). Se pueden clasificar en 4 grupos, según su mecanismo. En el primero tenemos a los relajantes directos del músculo liso (mebeverina, trimebutina, derivados de la papaverina), a priori los más «suaves», que actúan sobre las miofibrillas del músculo liso del intestino, reduciendo el tono y el peristaltismo sin alterar demasiado la motilidad. El más conocido es el Duspatalín (mebeverina). En este mismo grupo se incluyen las cápsulas de aceite de menta con cubierta entérica, que también han probado ser eficaces en la reducción del dolor abdominal, aunque pueden producir acidez/ardores y depresión respiratoria, por lo que están desaconsejadas en niños. En el segundo están los anticolinérgicos (butilhioscina, hioscina, hiosciamina, dicicloverina, belladonna -investigada en combinación con el fenobarbital– butilescopolamina, metescopolamina y bromuro de cimetropio), que atenúan los espasmos y contracciones del intestino inhibiendo la acción de la acetilcolina y reduciendo así el dolor abdominal (si está provocado por espasmos). Pueden tener más efectos secundarios (alteraciones visuales, retención urinaria, estreñimiento y sequedad de boca), aunque algunos como la Buscapina (butilescopolamina), el más conocido de este grupo, tienen menos por no actuar a nivel central (no atraviesa la barrera hematoencefálica). En el tercer grupo están los bloqueadores de los canales de calcio (bromuro de pinaverio, bromuro de otilonio, alverina, fenoverina, rociverina y pirenzepina), que previenen la entrada de calcio en las células del músculo liso del intestino, inhibiendo su actividad y provocando relajación intestinal. El más conocido de este grupo es el Spasmoctyl (bromuro de otilonio). El cuarto grupo son los antiespasmódicos usados en combinación (los anteriores con otros agentes como dimeticona o simeticona).
- Activadores de los canales de cloro: La linaclotida, aparte de su efecto laxante (contraindicada en SII-D), ha demostrado también un efecto inhibitorio sobre los nociceptores del colon, reduciendo el dolor abdominal en pacientes con SII-E. Eso sí, este efecto va apareciendo progresivamente, llegando a su zénit a las 4-10 semanas.
A menudo los fármacos anteriores no son efectivos o se quedan cortos, y en esta circunstancia se suele recurrir a neuromoduladores (fármacos que actúan sobre la actividad neuronal) como los antidepresivos, antipsicóticos, ansiolíticos, antiepilépticos, etc., que son medicaciones más fuertes, pero también más proclives a provocar efectos secundarios. Un artículo de 2017 en el American Journal of Gastroenterology, realizado por el expresidente de la Rome Foundation, Douglas Drossman, ofrece algunas sugerencias a los digestivos sobre las posibles combinaciones entre estos medicamentos a la hora de tratar trastornos funcionales digestivos que cursan con dolor. Otro artículo del mismo año y mismo autor principal, en Gastroenterology, nos aporta además un esquema con orientaciones generales:


En este otro artículo de la Rome Foundation se nos muestra en un sencillo esquema la afinidad de antidepresivos específicos con receptores de los distintos neurotransmisores. Si comparamos entre serotonina (5-HT) y norepinefrina/noradrenalina, hay que considerar que, aunque el esquema marque una afinidad similar en muchos casos, todos los antidepresivos que aparecen son más serotoninérgicos que noradrenérgicos, a excepción de nortriptilina, desipramina y milnaciprán (también la doxepina es más noradrenérgico de acuerdo a otras fuentes). El esquema puede ayudarnos a entender mejor algunos de los efectos secundarios a los que nos exponemos:
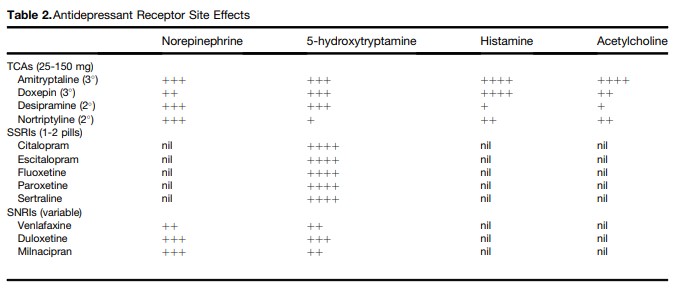
Notas a tener en cuenta:
- Los antidepresivos con mayor afinidad por receptores de norepinefrina/noradrenalina pueden provocar efectos secundarios como alteraciones del ritmo cardíaco, náuseas, cefaleas, ansiedad, hipertensión, leve estreñimiento… Y pueden ser útiles para el control del dolor.
- Los antidepresivos más afines a receptores de serotonina pueden provocar efectos secundarios como dolor de cabeza, mareos, somnolencia, disfunción sexual, aumento o disminución del apetito o del peso, leve diarrea… Y pueden mejorar síntomas anímicos comórbidos como ansiedad o depresión, sus efectos en el tratamiento del dolor no son muy significativos.
- Los antidepresivos más afines a receptores de histamina (disminuyendo los niveles o efectos de este neurotransmisor) serán más susceptibles de provocar sedación y aumento del apetito o del peso, entre otros.
- Los antidepresivos más afines a receptores de acetilcolina (disminuyendo los niveles o efectos de este neurotransmisor) generalmente serán susceptibles de provocar más estreñimiento, sequedad de boca, dificultad miccional, visión borrosa, aumento de la temperatura corporal, aumento de la presión sanguínea (Enciclopedia Britannica), y otros efectos secundarios anticolinérgicos.
Todo esto puede variar de paciente a paciente, incluso es posible tener efectos secundarios contrarios a los descritos, por lo que la opinión y experiencia clínica del profesional (y, desgraciadamente, la experimentación con distintos fármacos) es determinante a la hora de utilizar uno u otro.
En ocasiones, los antidepresivos y otros neuromoduladores (como los de los epígrafes inferiores) pueden provocar reacciones «paradójicas», empeorando los síntomas que supuestamente deberían tratar. Estas reacciones suelen desaparecer en 2-3 semanas máximo, pero a veces persisten y suelen ser un indicador de hipersensibilidad al fármaco. Se recomienda consultar al especialista URGENTEMENTE si la reacción no remite o los síntomas son intolerables.
Dicho esto, pasamos a los neuromoduladores.
- Antidepresivos: Tal como señala Lin Chang, digestivo experta en SII, miembro de la directiva de la Rome Foundation y del consejo asesor de la IFFGD, cuando el dolor es crónico y no va por «brotes» (para los que recomienda empezar por los antiespasmódicos), estaría indicado el uso de antidepresivos. Cuando se utilizan en dosis bajas (más bajas que las utilizadas para tratar la depresión), algunas veces reducen la intensidad de las señales de dolor que el intestino envía al cerebro. Al fin y al cabo, el 95% de la serotonina se produce en el intestino, donde actúa junto a otros neurotransmisores regulando la sensibilidad visceral, la motilidad y la secreción (alteradas en muchos casos de SII). Los antidepresivos actúan, así pues, regulando los niveles de neurotransmisores como la serotonina, la noradrenalina (el más importante en el dolor crónico), la acetilcolina o la dopamina. La mayoría pueden tener efectos secundarios sobre el deseo sexual, la concentración, el sueño, etc., algunos estriñen (tricíclicos especialmente), otros pueden, teóricamente, mejorar el estreñimiento (algunos Inhibidores Selectivos de la Recaptación de Serotonina)… lo recomendable es preguntar al médico sobre los pros y contras, aunque las reacciones de cada organismo ante un mismo antidepresivo pueden variar mucho. Los más utilizados en dolor crónico son los tricíclicos (amitriptilina, nortriptilina, melitraceno), algunos tetracíclicos (maprotilina) y los duales (duloxetina, venlafaxina), entre otros.
- Antipsicóticos: Los antipsicóticos suelen funcionar bloqueando los receptores D2 de dopamina, aunque algunos, como la quetiapina, también pueden aumentar la neurotransmisión noradrenérgica. A veces pueden utilizarse antipsicóticos atípicos (o de segunda generación) como la mencionada quetiapina o la sulpirida, que podrían mejorar el dolor y síntomas asociados del SII. En 2011, Drossman mostró datos preliminares en los que, en pacientes con SII severo o dolor abdominal mediado centralmente donde los antidepresivos por sí solos habían fallado, se añadía quetiapina en dosis de 25-100 mg junto a un antidepresivo, y al menos el 50% mantenían la medicación, y la mayoría reportaban beneficios, incluyendo pacientes que dejaron de tomarla. Otro de los más investigados en diversos trastornos de dolor crónico es la olanzapina, aunque la evidencia sigue siendo preliminar y no hay datos en SII. Los antipsicóticos actúan reduciendo o «regulando» los niveles de dopamina (clásicos/de primera generación), y a veces aumentan/reducen los de serotonina (los atípicos/de segunda generación). También pueden actuar sobre receptores adrenérgicos (de adrenalina/noradrenalina), muscarínicos (acetilcolina) y H1 (histamina, que aparte de sus funciones inmunitarias, también actúa como neurotransmisor). La pauta de estos fármacos, que suele ser una dosis baja, debe estar muy controlada por el especialista. Son frecuentes efectos secundarios como la sedación (quetiapina), el estreñimiento, o el aumento de peso (especialmente con olanzapina), entre otros.
- Benzodiazepinas: Los ansiolíticos más habituales. Actúan estimulando la neurotransmisión del GABA, el principal neurotransmisor inhibitorio de nuestro SNC, para lo cual se unen a la subunidad alfa del receptor GABA. Es habitual que se receten cuando existen trastornos de ansiedad acompañando al SII. Sus efectos sobre los síntomas del SII no están tan claros al haber pocos estudios (no existe ni un solo ensayo clínico aleatorizado, frente a los 18 ECAs con antidepresivos a fecha de 2018), aunque en la práctica clínica se utilizan con frecuencia. Ejemplos de benzodiazepinas son el alprazolam (sobre el que hay algún estudio), el lorazepam o el clonazepam. Estos fármacos pueden ser muy adictivos, aunque según un estudio de 2017, a las dosis empleadas en SII no lo serían tanto.
- Antiepilépticos: Dos de los más conocidos son la pregabalina (Lyrica) y la gabapentina (Neurontin), fármacos antiepilépticos que actúan sobre receptores benzodiazepínicos y a los que se les atribuye un potente efecto analgésico. Ambos fármacos reciben el nombre de «ligandos delta», debido a que se unen a la subunidad alfa-2-delta de los canales de calcio dependientes de voltaje (se abren/cierran según la carga iónica de la célula, es decir, el potencial de membrana) de tipo P/Q (pregabalina) o de tipo L (gabapentina) en las neuronas presinápticas sobreexcitadas (en este caso, enviando al cerebro señales de dolor), reduciendo la liberación de neurotransmisores excitatorios. Se ha dicho que estas moléculas imitan al GABA, el principal neurotransmisor inhibitorio del SNC (en contraposición al glutamato, el neurotransmisor excitatorio por excelencia), pero esto no está del todo claro, y un estudio de 2009 demostró que estos fármacos podrían actuar impidiendo la formación de nuevas sinapsis (el problema es que no sólo bloquearían sinapsis de señales dolorosas, sino todas, generando numerosos efectos secundarios). Se han hecho otras investigaciones en la línea de este último estudio que parecen confirmar la hipótesis, pero esto da para un debate extenso. Estos tratamientos, al igual que los antidepresivos o el resto de neuromoduladores, requieren supervisión médica, y su efectividad en el SII, sobre todo de la pregabalina, se ha empezado a investigar en los últimos años (aquí un ECA de 2016 con pregabalina, que pareció efectiva a dosis altas, de 450 mg/día). Los profesionales a veces los utilizan en casos muy severos, aunque no es habitual, sobre todo por la mala fama de estos fármacos en cuanto a efectos secundarios. No obstante, hay cierta evidencia, como este estudio de 2007 con pregabalina, de que sus efectos secundarios a largo plazo (26 semanas con 150-600 mg/día) podrían ser inferiores a los de antidepresivos como la venlafaxina o benzodiazepinas como el alprazolam.
- Antihistamínicos: La ciproheptadina, un antihistamínico de primera generación que parece actuar bloqueando receptores de serotonina, podría reducir los síntomas de dolor en trastornos funcionales digestivos como el SII, el dolor abdominal centralmente mediado, la migraña abdominal o la dispepsia funcional, aunque su efecto se ha estudiado casi exclusivamente en niños (estudio retrospectivo de 2016). Los efectos secundarios más frecuentes fueron el sueño/sedación y el aumento de peso.
- Opioides: Se usan cuando todo lo demás ha fracasado o cuando se trata de un dolor agudo y puntual. Apenas hay estudios específicos en SII. Se empezaría por la codeína para el dolor «moderado», el tramadol para el dolor «moderado a severo», la dihidrocodeína, hidrocodona, oxicodona o dextropropoxifeno para el dolor «severo», y la morfina y el fentanilo para momentos de dolor extremo. Estas medicaciones son potencialmente adictivas, por lo que sólo se pueden conseguir por prescripción médica. Los opioides pueden generar un estreñimiento muy severo, aunque hay medicaciones específicas para amortiguar este efecto secundario (naloxegol, metilnaltrexona, naldemedine). El uso de opioides en pacientes con SII o trastornos funcionales digestivos no está bien visto, por eso se usan en casos muy extremos o por breves periodos, y en algunos grupos de riesgo podría desembocar en un trastorno de dolor iatrogénico llamado «síndrome del intestino narcótico».
- Otros: Hay varios fármacos para los que no existe una evidencia científica sólida, pero que teóricamente podrían funcionar en el control del dolor visceral del SII. Entre ellos podemos mencionar la tizanidina, un derivado de la clonidina que actúa sobre los receptores α2-adrenérgicos (agonista).
Respecto a la duración del tratamiento, cuando se utilizan fármacos neuromoduladores como antidepresivos, antipsicóticos, antiepilépticos u opioides, se recomienda un tiempo mínimo de 6-12 meses, y JAMÁS se debe suspender de golpe sin antes consultar al médico, por la posibilidad de un síndrome de abstinencia/discontinuación. Los ansiolíticos, a diferencia de los anteriores, tienen efecto casi inmediato y no se aconsejan en tratamientos largos por su potencial adictivo, aunque esto puede depender de la persona, el problema a tratar y la dosis empleada.
A la hora de suspender un antidepresivo (aunque esto puede aplicarse a cualquier otro neuromodulador) que hemos mantenido durante un cierto tiempo, las guías clínicas a veces recomiendan una discontinuación lenta, con reducciones progresivas de la dosis durante 2-4 semanas hasta dejarlo del todo. Si no se hace así, puede aparecer un fenómeno llamado síndrome de discontinuación (o abstinencia, si hablamos de ansiolíticos), con síntomas muy variopintos que a veces se pueden confundir con recaídas. Sin embargo, algunos pacientes necesitan más tiempo, y, de hecho, estudios recientes en revistas de alto impacto (2019, 2020, 2020) van en esta misma línea, defendiendo una discontinuación más alargada en el tiempo y adaptada a las necesidades del paciente. Tanto los antidepresivos (síndrome serotoninérgico) como, más frecuentemente, los antipsicóticos (síndrome neuroléptico maligno, discinesia tardía) pueden provocar efectos secundarios muy desagradables que en el caso de los segundos podrían incluso permanecer tras dejar el fármaco, por no mencionar que en casos extremos pueden poner en peligro la propia vida (aunque esto cada vez es menos frecuente).
En cuanto a los procinéticos y antiespasmódicos, pueden utilizarse tanto a corto como a largo plazo, y se pueden suspender en cualquier momento.
NEUROESTIMULACIÓN Y TRATAMIENTOS INVASIVOS
Cuando las opciones anteriores fracasan, o hay limitaciones justificables que nos impiden probar ciertos medicamentos, tanto la Seguridad Social española como la sanidad privada, a través de las Unidades del Dolor, pueden ofrecer alternativas como la neuroestimulación, que consiste en alterar las señales cerebrales para disminuir la intensidad de los impulsos nerviosos que transmiten el dolor. La variante menos invasiva de neuroestimulación es la estimulación del nervio vago mediante dispositivos que se suelen colocar por fuera, generalmente en la oreja, a una determinada frecuencia y durante una serie de horas al día. El uso de esta tecnología en SII no es frecuente, aunque se están empezando a ver algunos avances, y en 2019 la FDA estadounidense autorizó el primer neuroestimulador específico para dolor abdominal funcional y SII (IB-Stim), que en este caso particular sólo está aprobado para adolescentes. Estas técnicas no están exentas de efectos secundarios, sobre todo cardíacos (el nervio vago controla funciones corporales como los latidos o la respiración), aunque no es lo habitual. El IB-Stim no actúa específicamente sobre el vago, sino que afecta a varios pares craneales relevantes en la transmisión del dolor. A día de hoy no esta á disponible en Europa, aunque sí hay otros dispositivos para la estimulación auricular del vago, como el TVNS Stimulator, eso sí, con poca o ninguna evidencia de su utilidad en SII.
Si este tipo de neuroestimulación no invasiva fracasa, hay otras técnicas mínimamente invasivas que pueden dar un alivio temporal (aunque a veces puede durar meses) y que se podrían hacer 2-3 veces al año (por anestesistas de una Unidad del Dolor). La única referencia que tenemos es un estudio de caso único de 2011, donde un paciente con dolor abdominal funcional (trastorno en el que el dolor, a diferencia del SII, no se asocia a eventos fisiológicos del intestino) obtuvo buenos resultados mediante un bloqueo nervioso en la zona, y se sometió posteriormente a una termocoagulación por radiofrecuencia del nervio esplácnico torácico, con efectos igualmente positivos que seguían presentes 3 meses después. Sin embargo, su indicación en SII no está totalmente clara, al no haber apenas estudios al respecto, por lo que consideramos que deben ser especialistas de Unidad del Dolor los que orienten al paciente en este sentido. Además, las lesiones sobre estos nervios podrían acarrear otros problemas, como pérdida de sensibilidad en otras zonas corporales (incluyendo genitales), y también comporta ciertos riesgos a largo plazo que hay que debatir con el médico.
El dolor en el SII se genera a través de un mecanismo donde intervienen tanto el intestino como el cerebro. En algunos pacientes el cerebro tendrá un mayor protagonismo. Esto no significa que los síntomas sean «psicológicos», sino que el procesamiento central del dolor está alterado, y aquí los neuroestimuladores auriculares del nervio vago podrían ser de utilidad (al menos hasta que opciones más sofisticadas como Neuralink/Grapheton avancen un poco más). En otros pacientes, el problema reside más en el propio intestino/abdomen, y un bloqueo a esa altura podría tener más eficacia. Sin embargo, las estrategias de control del dolor podrían ser útiles independientemente del origen del mismo, por lo que vale la pena intentarlas todas, siempre con supervisión médica.
SUPLEMENTOS**
- Probióticos: La evidencia disponible sobre ellos es muy pobre, existen numerosos estudios pero su potencia estadística es muy cuestionable. Hay algunos probióticos que tienen un nivel de evidencia superior al resto (revisión de 2017), como la cepa Bifidobacterium Infantis 35624 (Alflorex) o la cepa Lactobacillus Plantarum 299v (DSM 9843) (ProTransitus), las cuales han mostrado efectos sobre el dolor, la hinchazón, o las alteraciones en la defecación de algunos pacientes con SII. Si un probiótico se deja de tomar, los síntomas suelen reaparecer. Y aunque funcionen, apenas hay datos sobre la duración de sus efectos terapéuticos (más allá de 4-8 semanas la mayoría de las veces). Si se prueban, deben mantenerse durante aproximadamente un mes para apreciar cambios, y es normal que los primeros días den más efectos secundarios. Si éstos no remiten o son intolerables, se recomienda dejar de tomarlos o probar con uno diferente. Deben evitarse, al menos de primeras, todos los que lleven prebióticos (el PRObiótico es la cepa con la bacteria, el PREbiótico es el sustrato que se añade para que ésta prolifere) añadidos, tales como fructo/galactooligosacáridos o inulina, que nos producirán gases, los cuales en el SII son muy mal tolerados.
- Procinéticos: El IberoGast ha conseguido resultados favorables en el tratamiento del dolor abdominal, así como en los síntomas generales del SII. Sin embargo, el nivel de evidencia es todavía muy pobre, y lleva componentes con alto contenido en FODMAPs como la manzanilla, que podrían sentar mal a algunos pacientes.
- Silicatos de aluminio/magnesio: La diosmectita (Megasmect), un tratamiento utilizado especialmente en SII-D por su efecto astringente (contraindicada en SII-E), podría ayudar al dolor, aunque la evidencia al respecto es pobre.
HÁBITOS
Cuando los dolores son incontrolables y el resto de medicinas no dan resultado, una fuente de calor contra el vientre puede servir como alivio momentáneo (si la usamos para dormir, deben emplearse dispositivos que se apaguen automáticamente o que no supongan un riesgo durante el sueño). En Amazon hay un buen repertorio de bolsas de agua caliente, y también mantas eléctricas que funcionan mediante un sistema eléctrico y que pueden apagarse automáticamente, evitando quemarnos la piel. Del mismo modo, podemos usar parches de calor como los que se emplean en el dolor lumbar (hay marcas como Thermacare o Voltatermic), y con los cuales las quemaduras son muy poco frecuentes. Según la cualidad del dolor, a veces puede ser más conveniente usar bolsas de hielo (bolsas con un gel refrigerante que van en una funda y pueden mantenerse congeladas durante horas), pues el calor puede no irle bien a todo el mundo.
* Con la etiqueta «medicamentos» nos hemos referido a tratamientos que, por su estatus legal/sanitario, son fármacos consolidados, cuya eficacia y perfil de seguridad han sido contrastados.
** Con la etiqueta «suplementos» nos hemos referido a tratamientos que, por su estatus legal/sanitario, son fármacos poco consolidados, de eficacia y seguridad no contrastadas.
