El eje intestino-cerebro
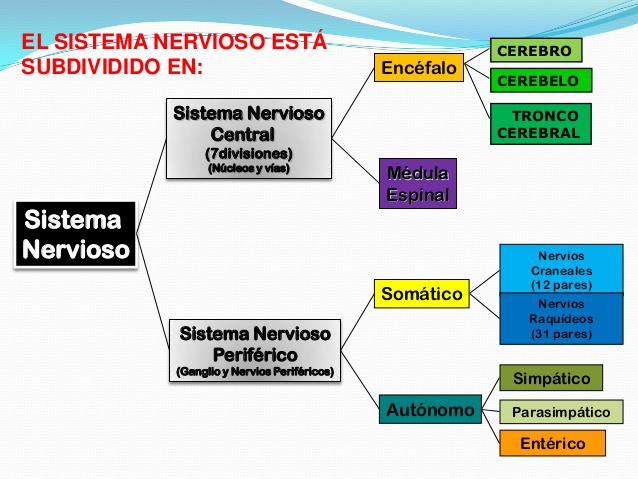
El sistema nervioso del intestino recibe el nombre de Sistema Nervioso Entérico. Es una subdivisión del Sistema Nervioso Autónomo (Simpático, Parasimpático, Entérico), que a su vez es una subdivisión del Sistema Nervioso Periférico (Sistema Nervioso Autónomo y Sistema Nervioso Somático). Como una imagen vale más que mil palabras:
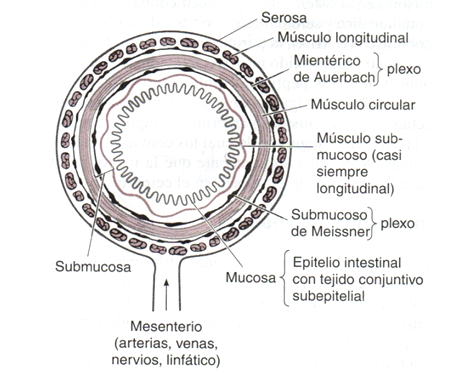
Más abajo tenemos un corte transversal del intestino, en el que podemos observar las estructuras del SNA Entérico. Ascendiendo por la pared externa del intestino estaría el nervio vago, que llega hasta el Sistema Nervioso Central, siendo la conexión principal entre ambos. El SNA Entérico se expande desde el esófago hasta el colon, ambos inclusive. Todas estas zonas estarían, así pues, comunicadas con el cerebro a través del nervio vago, aunque éste no llega a contactar con el lumen (los alimentos, bacterias y otros microorganismos que viven en el interior del tubo digestivo) directamente, pero si indirectamente a través de las células enteroendocrinas, como vimos en el apartado sobre microbiota.
En el vídeo inferior se nos da una explicación general del rol del SNA Entérico. Es importante tener en cuenta que, aunque el intestino reciba el sobrenombre de «segundo cerebro», la realidad es que «sólo» tiene 100 millones de neuronas, frente a los 86.000 millones del cerebro. Es decir, aunque es el segundo órgano con más neuronas, tiene 860 veces menos que el primero, una diferencia considerable.
En este otro vídeo, en inglés, tenemos una explicación algo más detallada de cómo el Sistema Nervioso Entérico (SNE en adelante) regula la motilidad en personas sanas y con SII:
Para los no angloparlantes, podemos resumirlo en que, a lo largo de todo el intestino (delgado y grueso), tenemos unas neuronas sensoriales (2012) en los plexos submucoso (Meissner) y mientérico (Auerbach) que, mediante las vías neuronales ascendentes y descendentes (donde las células enteroendocrinas actúan como mediadoras entre el lumen intestinal y el SNE), van dando órdenes a los músculos circular y longitudinal para que se contraigan y relajen según convenga (como se explica al principio del apartado sobre motilidad), proceso en el que también colaboran los sistemas nerviosos simpático y parasimpático (que completan junto al SNE el sistema nervioso autónomo). Un neurotransmisor esencial en este proceso es la acetilcolina (por eso los fármacos anticolinérgicos/antimuscarínicos, que bloquean su mecanismo de acción, pueden inducir una disminución de la motilidad). La serotonina, aunque menos, también estimula la motilidad, de ahí que en ocasiones puntuales se hayan propuesto para pacientes con TFD de tipo estreñimiento (2017). Y otro que también tiene cierta relevancia es la noradrenalina, que puede ralentizar la motilidad (2011), de ahí que a veces se utilicen ISRN para buscar un efecto astringente (2017).
Una de las estructuras clave del eje intestino-cerebro es el nervio vago. Éste es el nervio principal del Sistema Nervioso Autónomo Parasimpático (y completa el SNA con el parasimpático y el entérico), y tiene un 80% de fibras aferentes (información que llega al cerebro desde los órganos) y un 20% de fibras eferentes (información que llega a varios órganos desde el cerebro) (2018). El nervio vago ha sido considerado como “el sexto sentido” por su rol en la conciencia interoceptiva (2017). Inerva áreas del oído, epiglotis, músculo de la deglución, esófago, corazón, bronquios, hígado, páncreas, riñones y vísceras abdominales. En la parte que nos interesa, recorre todo el tracto digestivo desde el inicio hasta el ángulo esplénico del colon (esto último no se sabe con precisión, pero es un hecho que inerva gran parte del colon). En el video en inglés sobre el SNA Entérico que hemos visto más arriba se explica en detalle cómo las fibras aferentes del nervio vago se insertan en todas las capas del tracto digestivo, en los plexos submucoso y mientérico (no llega a atravesar la capa epitelial, por lo que no tiene contacto directo con el lumen/interior del tubo digestivo) (2007).
El nervio vago tiene propiedades antiinflamatorias (2018) mediadas a través de sus fibras tanto aferentes como eferentes. También se le ha atribuido en algunos estudios (2018) un efecto protector de la barrera intestinal, y se especula con que una disminución en su actividad podría asociarse con un aumento de los procesos inflamatorios, y en consecuencia, un aumento de la permeabilidad intestinal.
En los cuadros funcionales como el SII, así como en la Enfermedades Inflamatorias Intestinales, el nervio vago parece tener un tono disminuido (2016). Su restauración y el efecto que esto podría tener en los síntomas es una de las líneas de investigación en el tratamiento de estas patologías. De hecho, el estrés, que empeora los síntomas en ambas condiciones, tiene una acción inhibitoria sobre el nervio vago (y, por ende, sobre el SNA parasimpático) y estimulante sobre el SNA simpático, todo lo cual favorecería los procesos inflamatorios.
Finalmente, y para cerrar esta introducción al eje intestino-cerebro, el SNE tiene un papel clave en la hipersensibilidad visceral, que, cuando pasa al SNC, provoca sensaciones de dolor, hinchazón y molestia. Este tipo de sensaciones son creadas por el cerebro con los inputs recibidos del cuerpo, es importante recordar que la hipersensibilidad visceral no las provoca por sí sola, debe pasar al SNC para ello.
El por qué de esta hipersensibilidad visceral, y el por qué del dolor, o de las alteraciones de la motilidad, es la pregunta que todos los investigadores de SII se hacen. En los apartados de alteraciones inmunitarias, alteraciones psicosociales/eje HPA y alteraciones de la microbiota podemos encontrar algunos mecanismos alterados que podrían explicar en parte los síntomas. Aquí profundizaremos en las alteraciones puramente neurológicas que, pudiendo ser una consecuencia de los anteriores o no, se asocian frecuentemente a los síntomas de pacientes con SII.
